Problemi Risolti
inserita 09-05-2020
Resa di Reazione
problema 2
“ Esempi di problemi risolti di resa di reazione „
La teoria sulla resa di reazione e sulla risoluzione dei problemi la trovate in questo post Calcoli Stechiometrici - la resa di reazione..
Risolviamo il seguente problema
PROBLEMA: 2 - La fermentazione del glucosio in ambiente anaerobico può portare alla formazione di etanolo (un alcol) secondo la seguente reazione
sapendo che la resa percentuale è dell'87% calcola:
a - la massa i grammi di etanolo che si ottiene da 800 grammi di glucosio
b - quanti grammi di glucosio sono necessari per ottenere 550 grammi di alcol.
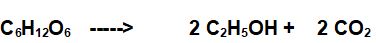
PUNTO A
Dal post precedente Reazioni di sintesi (1) sappiamo che questa è una semplice reazione di sintesi di un sale binario facile da bilanciare.
(l'alluminio sta al III gruppo e cede in blocco i suoi 3 elettroni di valenza, il Bromo necessita di un solo elettrone per cui il sale che si forma, il bromuro di alluminio ha i 2 elementi in rapporto di 1:3.
Per la domanda A noi sappiamo, oltre alla resa percentuale che ci fornisce il testo dell'esercizio, la quantità di partenza di glucosio: 800 grammi.
Quindi possiamo calcolare con la tabella la RESA TEORICA RT
TAPPA 1 IMPOSTIAMO LA TABELLA E CALCOLIAMO LE QUANTITA':

Quindi TEORICAMENTE, se la reazione fosse al 100% otterrei 409,10 grammi di Etanolo.
Ma la reazione ha una resa percentuale dell'87% quindi in base alla relazione:
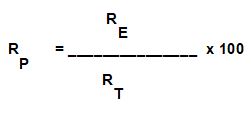
RE=RP*RT/100 = 355,92 grammi di prodotto ottenuto
PUNTO B
Per la domanda B noi vogliamo sapere quanti grammi di glucosio servono per ottenere 550 grammi di Etanolo.
Oltre alla resa percentuale che ci fornisce il testo dell'esercizio conosciamo quindi la RESA EFFETTIVA RE
TAPPA 1 - CALCOLIAMO LA RESA TEORICA:
RT=RE*100/RP = 632,18 grammi di prodotto
Per cui devo mettere a reagire una quantità di glucosio come se volessi ottenere teoricamente 632,18 grammi di etanolo, in quanto il 13% va perduto per vie ineluttabili durante la reazione.
TAPPA 2 - CALCOLIAMO LA QUANTITA' DI GLUCOSIO NECESSARIO:
Usiamo la tabella come al solito vedi IL POST SUI CALCOLI STECHIOMETRICI
In questo caso partiamo dal prodotto che conosciamo e ci ricaviamo il reagente

Calcoliamo il numero di moli del prodotto

Ora dai coefficienti stechiometrici sappiamo che per ogni 2 moli di etanolo basta 1 mole di glucosio, per cui devo dividere a metà il numero di moli di etanolo per ottenere le moli di glucosio che hanno reagito.
13,72/2=X/1

Moltiplico per la massa molare e ottengo il risultato.
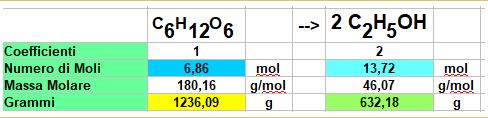
Quindi per ottenere 550 grammi di etanolo devo mettere a reagire 1236,09 grammi di glucosio, dato che la reazione ha una resa percentuale dell'87%
