Le concentrazioni percentuali
Le tre concentrazioni percentuali m/m m/V V/V
inserita il 26-03-2023
Definizione di concentrazione percentuale
“ Le concentrazioni percentuali esprimono la quantità di soluto in una qualsiasi miscela „
In altre pagine abbiamo definito le unità di misura della concentrazione che si basano sul numero di moli di soluto in una soluzione: La Molarità e la molalità.
E abbiamo risolto alcuni esercizi di calcolo di tali concentrazioni e come convertire l'una nell'altra.
- esercizi svolti sulla molarità (1)
- esercizi svolti sulla molarità (2)
- esercizi svolti sulla molalità (1)
- esercizi svolti sulla molalità (2)
- esercizi svolti sulla molalità (3)
- esercizi svolti da molarità a molalità
- esercizi svolti da molalità a molarità
In questa pagina definiamo un gruppo di concentrazioni concettualmente diverse e di uso più generale: le concentrazioni percentuali.
Sono sostanzialmente due le differenze tra queste concentrazioni e molarità e molalità
- 1- Sono di uso più ampio. Si possono applicare non solo alle soluzioni ma a qualsiasi miscela o miscuglio, anche eterogenei. Per questo si usano in svariati campi non solo in chimica
- 2- Non necessitano del calcolo del numero di moli ma si misura o pesa direttamente la quantità di soluto in massa o in volume.
Quante sono le concentrazioni percentuali?
Le concentrazioni percentuali sono sostanzialmente 3:
- 1- Concentrazione massa su massa %m/m
- 2- Concentrazione massa su Volume %m/V
- 3- Concentrazione Volume su Volume %V/V
Per cui si esprimono in rapporti 1 su 1 milione o 1 su un miliardo utilizzando le appropriate unità di misura
(ad es mg (soluto)/Kg (soluzione) --> 1/1000000)
Le concentrazioni percentuali sono di lettura immediata e di uso pratico. Sono per esempio ampiamente usate in alimentazione. Nelle etichette degli alimenti quello che leggiamo sono proprio le concentrazioni percentuali che ci permettono immediatamente di sapere la quantità di carboidrati, grassi, proteine, sale o altro che sto ingerendo quando mangio 100 grammi o bevo 100 millilitri di alimento o bevanda, oppure quanto ne contiene un singolo pezzo (ad es. un biscotto).
Per cui a lezione le associo allo studio della corretta alimentazione nelle ore dedicate all'educazione civica.
La figura qui sotto compara le tre concentrazioni percentuali che hanno la stessa formulazione matematica.

Vediamole adesso una per una. Nelle pagine successive vedremo come risolvere degli esercizi sulle concentrazioni percentuali.
La concentrazione percentuale massa su massa
Percentuale in massa (% m/m):
Questa unità di misura indica la quantità di una sostanza presente in una soluzione o miscela rispetto alla massa totale della soluzione o miscela stessa.
Il riferimento è 100 grammi di soluzione/miscuglio
Si usa per soluzioni, miscugli o prodotti in cui sia il soluto che la soluzione sono allo stato solido.

Ad esempio, una soluzione al 5% m/m di sale significa che ci sono 5 grammi di sale in 100 grammi di soluzione.
Questa concentrazione è quella riportata nelle etichette alimentari di informazione nutrizionale. Prendiamo ad esempio l'etichetta della figura sotto che si riferisce a dei biscotti in commercio.
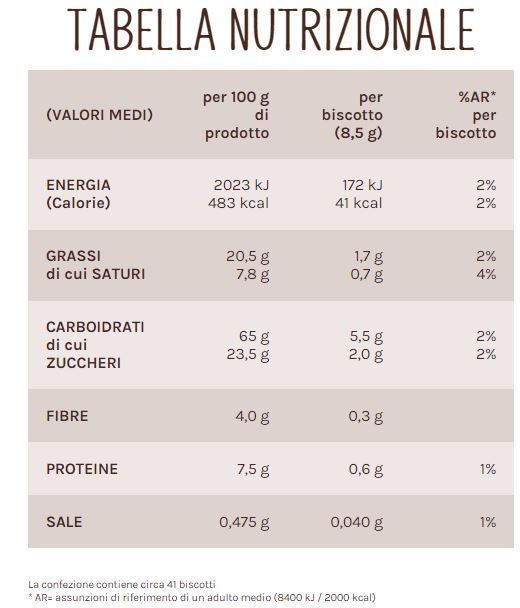
Le etichette di informazioni nutrizionali hanno sempre due colonne: per 100 grammi, la formulazione classica della concentrazione
% massa/massa e per pezzo, che mi permette di sapere quanti nutrienti assumo per ogni biscotto in questo caso.
Quindi in questo caso assumendo 100 grammi di biscotti assumo:
20,5 grammi di grassi - miscuglio solido al 20,5 % m/m
65 grammi di carboidrati - miscuglio solido al 65 % m/m
Di questi carboidrati ben 23,5 grammi sono zuccheri semplici - miscuglio solido al 23,5 % m/m
7,5 grammi di proteine - miscuglio solido al 7,5 % m/m
4 grammi di fibre - miscuglio solido al 4 % m/m
0,475 grammi di sale - miscuglio solido al 0,5 % m/m
Quantità molto elevate di grassi e zuccheri semplici ma dobbiamo considerare che non mangiamo ovviamente 100 grammi di biscotti a colazione.
Nella seconda colonna avete già calcolata la quantità per ogni biscotto, per cui è semplice capire quanto si assume di ogni singolo nutriente.
La concentrazione percentuale massa su Volume
Percentuale massa su Volume (% m/V):
Questa unità di misura indica la quantità di una sostanza in grammi presente in una soluzione o miscela rispetto al volume totale della soluzione o miscela stessa.
Il riferimento è 100 millilitri di soluzione/miscuglio

Ad esempio, una soluzione al 5% m/v di glucosio significa che ci sono 5 grammi di glucosio in 100 millilitri di soluzione.
Si usa per soluzioni, miscugli o prodotti in cui il soluto è solido e la soluzione è invece allo stato liquido.
Come esempio di questa concentrazione possiamo considerare la quantità di zucchero presente in alcune bevande
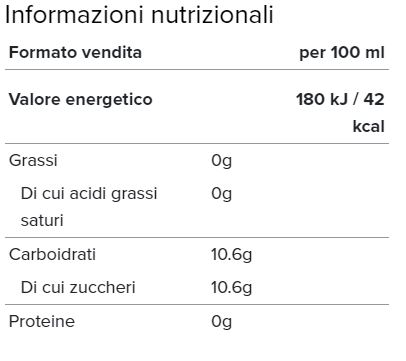
Le bevande gassate sono fatte essenzialmente di acqua e zucchero, con tracce di aromi.
è molto più facile eccedere in questo caso rispetto ai biscotti menzionati in precedenza
l'etichetta ci informa che:
bevendo 100 millilitri di bevanda assumo:
10,6 grammi di carboidrati, tutti zuccheri semplici - miscuglio liquido al 10,6 % m/V
Considerate che una lattina contiene 330 mL. Non è difficile capire che anche consumare una lattina al giorno implica l'assunzione di una quantità di zuccheri esagerata per l'organismo.
La concentrazione percentuale Volume su Volume
Percentuale Volume su Volume (% V/V):
Questa unità di misura indica la quantità di una sostanza presente in una soluzione o miscela rispetto al volume totale della soluzione o miscela stessa.
Il riferimento è 100 millilitri di soluzione/miscuglio

Ad esempio, una soluzione al 5% v/v di etanolo significa che ci sono 5 millilitri di etanolo in 100 millilitri di soluzione.
Si usa per soluzioni, miscugli o prodotti in cui sia il soluto sia la soluzione sono allo stato liquido.
La percentuale in volume è spesso utilizzata in chimica analitica e in enologia per misurare la concentrazione di alcol. Prendiamo come esempio alcune bevande alcoliche generiche.
Per le bevande alcoliche la concentrazione percentuale V/V di alcool nella bevanda è riportata direttamente sull'etichetta come gradazione alcolica.
per cui
l'etichetta potrebbe ad esempio informarci che:
bevendo 100 millilitri di bevanda assumo:
una birra leggera: gradazione alcolica 4,7 % - 4,7 millilitri di etanolo ogni 100 millilitri di bevanda
vino medio: gradazione alcolica 12 % - 12 millilitri di etanolo ogni 100 millilitri di bevanda
una grappa o altri superalcolici: gradazione alcolica 47 % - 47 millilitri di etanolo ogni 100 millilitri di bevanda
Per cui la quantità di alcool contenuta in 100 milllilitri di bevanda può variare anche più di 10 volte a seconda del tipo di prodotto!
Per calcolare l'effettiva quantità di alcool assunto e le conseguenze di tale assunzione sull'organismo bisogna poi convertire i millillitri in grammi di sostanza, ma lo faremo nelle pagine seguenti in cui svolgeremo alcuni esercizi di varia difficoltà sulle concentrazioni percentuali.
Pagina precedente -esercizi svolti sulla molarità e molalità
Pagina successiva -esercizi svolti sulla % massa su massa
Concentrazioni delle soluzioni chimiche
Calcolo della Molarità, delle moli e Numero di Avogadro - teoria e calcolatore online
molalità e concentrazione molale
esercizi svolti sulla molarità (1)
esercizi svolti sulla molarità (2)
esercizi svolti sulla molalità (1)
esercizi svolti sulla molalità (2)
esercizi svolti sulla molalità (3)
esercizi svolti da molarità a molalità
esercizi svolti da molalità a molarità
Le concentrazioni percentuali m/m esercizi svolti (1)
Le concentrazioni percentuali m/V esercizi svolti (2)
Le concentrazioni percentuali V/V esercizi svolti (3)
Altri argomenti di chimica
Il bilanciamento di reazioni chimiche
Altri convertitori
Calcolo della Molarità, delle moli e Numero di Avogadro - teoria e calcolatore online
tabelle
tabelle riassuntive su Mercurio
tabelle riassuntive su Plutone
Apps e Test
