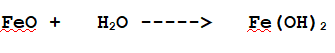reazioni di sintesi problemi risolti (2)
inserita 08-02-2021
Problemi risolti
5- Scrivi le reazioni di sintesi che trasformano il Calcio metallico in:
“ Per la teoria sulle reazioni di sintesi consultate i post: reazioni di sintesi (1) e (2) e Reazioni di sintesi - problemi risolti (1) „
Scrivi le reazioni di sintesi che trasformano il Calcio metallico in:
A- Ossido di Calcio
B- Cloruro di Calcio
C- Idruro di Calcio
D- Nitruro di Calcio
Sono tutte reazioni molto semplici.
Il Calcio metallico, che non si trova in natura in quanto è un elemento molto reattivo ed è sempre combinato con altri elementi, ma si può ottenere in laboratorio, entra in reazione un atomo alla volta. I 4 non-Metalli invece sono tutti biatomici.
Nel caso A si forma un Ossido Basico. Negli altri tre casi invece sono tutti sali binari.
Impostiamo le semireazioni e risolviamo:
ricordiamo che:
Il Calcio è al secondo gruppo e può donare e dona 2 elettroni.
A- l'Ossigeno è al sesto gruppo e ha bisogno di 2 elettroni per completare l'ottetto.
B- Il Cloro è al settimo gruppo e ha bisogno di 1 elettrone per completare l'ottetto.
C- Lo Iodio è al settimo gruppo e ha bisogno di 1 elettrone per completare l'ottetto.
D- l'Azoto è al quinto gruppo e ha bisogno di 3 elettroni per completare l'ottetto.
L'Ossigeno forma l'Ossido di Calcio.
Azoto, Cloro e Iodio, formano rispettivamente: Nitruro di Calcio, Cloruro di Calcio, Ioduro di Calcio.
per cui impostiamo le semireazioni, il composto finale (giusto equilibrio tra elettroni ceduti e ricevuti) e bilanciamo
A- Ca + O2 -----------> ...............................
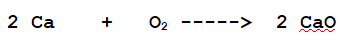
B- Ca + Cl2 -----------> ...............................
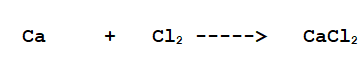
C- Ca + I2 -----------> ...............................

D- Ca + N2 ------------> ................................
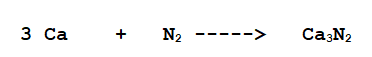
6- Completa le seguenti reazioni di sintesi attribuendo il nome ai composti che si formano.
“ Semireazioni di formazione di sali binari e idruri covalenti „
(basatevi sulle spiegazioni dell'esercizio precedente per i primi 2; il Sodio Na è un metallo del primo gruppo e il Magnesio Mg un metallo del secondo gruppo; si sintetizzano sali binari, Cloruro di Sodio e Cloruro di Magnesio); Nel punto C invece si forma un idruro covalente molto famoso: l'Ammoniaca)
A- Na + Cl2 -----------> ...............................
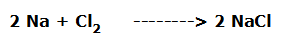
B- Mg + Cl2 -----------> ...............................
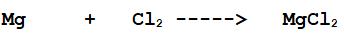
C- N2 + H2 ------------> ................................
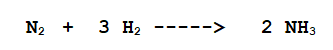
7- Scrivi e bilancia le reazioni di sintesi dei seguenti prodotti:
“ in questi esercizi si deve impostare l'intera reazione a partire dal nome del prodotto „
Per risolvere questo tipo di esercizi bisogna considerare le proprietà dei singoli elementi, oppure considerare i meccanismi di reazione di ossidi basici o anidridi con acqua. (vedi teoria)
A Triossido di Zolfo.
LINEE GUIDA:
Elementi che reagiscono, ovviamente Zolfo e Ossigeno.
Lo Zolfo è ottatomico l'Ossigeno biatomico.
Il composto è comunemente noto come anidride Solforica
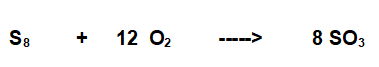
B Fluoruro di Idrogeno.
LINEE GUIDA:
Elementi che reagiscono ovviamente Fluoro e Idrogeno.
Il Fluoro è biatomico l'Idrogeno biatomico.
Il composto è comunemente noto come Acido Fluoridrico
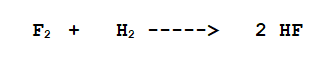
C Idrossido di Calcio.
LINEE GUIDA:
Reazione di formazione di un idrossido.
Reagiscono un Ossido Basico e Acqua.
In questo caso Ossido di Calcio CaO.
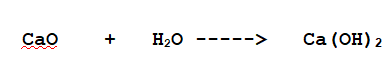
D Ossido di Bario.
LINEE GUIDA:
Elementi che reagiscono ovviamente Bario e Ossigeno.
Il Bario è un metallo del II gruppo, l'Ossigeno è biatomico
Il composto che si forma è un Ossido Basico
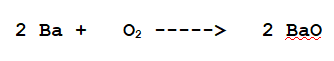
E Bromuro di Potassio.
LINEE GUIDA:
Elementi che reagiscono ovviamente Bromo e Potassio.
Il Potassio è un metallo del I gruppo, il Bromo è un alogeno del settimo gruppo
Il composto che si forma è un Sale Binario

F Idruro di Litio.
LINEE GUIDA:
Elementi che reagiscono ovviamente Idrogeno e Litio.
Il Litio è un metallo del I gruppo, l'Idrogeno è un non-Metallo del primo gruppo
Il composto che si forma è un Idruro metallico
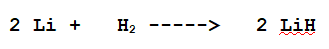
G Acido Nitrico.
LINEE GUIDA:
L'Acido Nitrico è un ossiacido: si forma quindi dalla reazione dell'acqua con la rispettiva Anidride, l'anidride Nitrica.
L'Azoto, al quinto gruppo ha il numero di ossidazione massimo, +5 sia nell'anidride che nell'acido.
Il composto che si forma è un ossiacido
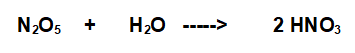
H Idrossido di Ferro (II).
LINEE GUIDA:
L'Idrossido di Ferro (II) è un Idrossido: si forma quindi dalla reazione dell'acqua con il rispettivo Ossido Basico.
Dato che il numero tra parentesi ci indica il numero di Ossidazione del Ferro, +2, ogni atomo di Ferro mette a disposizione 2 elettroni sia nell'Ossido che nell'Idrossido.
E dato che il Ferro può assumere +2 e +3, l'Ossido si chiama Ossido Ferroso e l'Idrossido Idrossido Ferroso, nella nomenclatura tradizionale